Traiter le diabète par une transplantation de cellules insulino-sécrétrices ?
Pierre Yves Benhamou
Diabétologie, CHU de Grenoble
La recherche thérapeutique en matière de diabète vise le même objectif général: prévenir les complications chroniques et invalidantes de la maladie, au prix d'un traitement offrant des contraintes quotidiennes minimales, une sécurité maximale et une qualité de vie optimale. On sait depuis quelques années que cet objectif passe par l'obtention d'une glycémie la plus normale possible, le plus tôt possible et le plus longtemps possible. La transplantation de tissu endocrine, capable de sécréter de l'insuline en réponse au glucose, est en mesure de réaliser cet objectif chez les diabétiques de type 1. Des îlots allogéniques infusés dans le foie survivent, sécrètent de l'insuline, permettent une amélioration significative du contrôle glycémique, voire un sevrage de l'insulinothérapie pendant des périodes allant de quelques semaines à quelques années, sans morbidité directe, mais au prix d'une immunosuppression lourde. Les défis à relever sont triples : améliorer la reproductibilité de la procédure ; réduire la toxicité du traitement immunosuppresseur ; trouver une source de tissu permettant de faire face à la demande : 200000 diabétiques insulino-dépendants en France, plus de 15 millions dans le monde.
Les Aspects Techniques
L'îlot pancréatique est une structure grossièrement sphérique, mesurant 50 à 500 µm, composé d'un bon millier de cellules dont la majorité, les cellules ß, sécrètent de l'insuline, et représenté au nombre d'environ 1 million dans un pancréas humain adulte, soit à peine 1% de la glande pancréatique. Le pancréas prélevé minutieusement chez un donneur en état de mort cérébrale doit être transporté dans un délai de 8 heures vers le laboratoire d'isolement à 4ºC. L'expérience acquise depuis 1990 a permis d'identifier certains critères chez le donneur (poids, âge, glycémie, hémodynamique) permettant de prédire la qualité et le rendement des îlots, mais la valeur prédictive de ces critères demeure limitée. La coexistence fréquente de programmes de greffes de pancréas et de greffes d'îlots est un facteur limitant la disponibilité d'organes de qualité pour l'isolement des îlots. L'étape de digestion du pancréas consiste à dissocier les îlots des autres tissus constitutifs du pancréas. Cette digestion s'effectue en une trentaine de minutes à l'aide d'une enzyme, la collagénase, qui reste difficile à produire avec une qualité reproductible. Cela contribue à rendre difficilement prévisible le nombre d'îlots obtenu à partir d'un pancréas donné. Le produit de digestion ainsi obtenu doit alors être purifié. Pour ce faire, on a affaire à une centrifugation, permettant de trier les tissus en fonction de leur densité propre. On aboutit ainsi à une préparation pure constituée à 95% d'îlots pancréatiques, et représentant un volume de tissu d'à peine 5 à 15 cm3. Ces îlots peuvent être soit mis en culture pendant 8 à 15 jours, soit congelés, soit transplantés d'emblée.
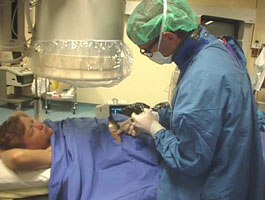
La transplantation proprement dite est l'étape la plus simple. Les îlots purifiés sont remis en suspension dans 50 ml de milieu de survie et infusés chez le receveur en 15 à 30 minutes dans la veine porte, abordée sous anesthésie locale par ponction transhépatique sous contrôle échographique. La tolérance du geste est parfaite. Les îlots vont ainsi se disperser dans le flux sanguin hépatique et s'implanter dans le foie. Au bout de quelques heures à quelques semaines, les îlots libèrent l'insuline en réponse au glucose. Pour ce faire, ils auront dû franchir de nombreux obstacles: préservation d'une bonne viabilité, acquisition d'une vascularisation propre, résistance à l'inflammation, au rejet de greffe, à la récidive de la maladie autoimmune à l'origine du diabète, ou à la toxicité des médicaments anti-rejet. La recherche actuelle vise à réduire ces obstacles.
La masse de tissu greffé est un des principaux facteurs prédicteurs de succès : une masse de 6000 à 10000 îlots/kg de receveur est requise, pouvant être obtenue à partir d'un seul pancréas, mais nécessitant parfois de combiner les îlots de deux glandes voire plus.
Les Résultats Actuels
Le Registre International des Greffes d'Ilots fait état de 267 allogreffes d'îlots chez des receveurs atteints de diabète de type 1 entre le 1.1.90 et le 31.12.98. Le taux d'insulino-indépendance dépassant un an post-greffe est de 8% (20 patients dans le monde), la plus longue durée de sevrage insulinique rapportée est de 70 mois. La fonctionnalité du greffon, attestée par un taux de C-peptide à 0.5 ng/ml, est de 35% à un an. Entre les mains des meilleures équipes (Giessen, Milan, Bruxelles, Miami, Genève), le taux d'insulino-indépendance passe à 18 %, tandis que 51% des greffons produisent de l'insuline pendant au moins un an, permettant d'améliorer sensiblement l'équilibre métabolique et le confort du traitement et de réduire le risque hypoglycémique, même si le patient doit continuer ses injections d'insuline. La greffe d'îlots demeure donc une thérapeutique de recherche clinique, nécessitant un investissement organisationnel lourd contrastant avec la simplicité du geste, susceptible dans 1/3 à 1/2 des cas de restaurer une insulinosécrétion. Une quarantaine d'équipes dans le monde ont recouru à la greffe d'îlots ; en France, deux programmes sont en cours, dans la région lilloise d'une part, dans la région Rhône-Alpes et Est d'autre part.
Les Orientations de la Recherche
Si les 20 patients sevrés d'insuline grâce à une greffe d'îlot témoignent de la réalité d'une thérapie cellulaire du diabète, un problème est la faible reproductibilité de la procédure. A l'heure actuelle, la maîtrise des phénomènes de rejet d'allogreffe et de récurrence de l'autoimmunité diabétique fait appel à une immunosuppression conventionnelle (inhibiteurs de calcineurine type ciclosporine ou FK506, stéroïdes, MMF). De ce fait, la greffe d'îlots reste cantonnée aux patients diabétiques de type 1 parvenus à un stade évolué de leur maladie, l'insuffisance rénale terminale : la meilleure indication est le patient porteur d'un greffon rénal fonctionnel seul, et ayant un greffon pancréatique soit absent, soit non fonctionnel. Or cette immunosuppression est peu efficace pour maîtriser l'autoimmunité, et de surcroît elle est toxique pour l'îlot. On attend beaucoup de nouveaux agents immunomodulateurs, non diabétogènes, sur le point d'être testés en clinique. Les données expérimentales animales établies avec l'un d'eux, l'anticorps anti-CD40L Antova, sont très prometteuses. Grâce à cet agent, on espère proposer la greffe à des diabétiques à un stade plus précoce de leur maladie. La recherche d'un site de greffe plus adapté que le site hépatique est également une clé importante. La résolution du problème de la reproductibilité et de la toxicité de l'immunosuppression est l'étape qui fera véritablement décoller la greffe d'îlots. La quasi-totalité des greffes d'îlots réalisées dans le monde sont des allogreffes de tissu adulte. L'étape ultérieure devra s'attacher à définir la source optimale de tissu endocrine insulino-sécréteur. Le porc est proposé de longue date comme une source potentielle d'îlots intéressante. Cependant, l'enjeu actuel est de démontrer l'innocuité sur le plan microbiologique d'une greffe de tissu porcin. D'autres équipes s'attachent à mettre au point une lignée cellulaire à prolifération et différenciation contrôlables, capable d'insulinosécrétion régulable par le glucose. Ces cellules seraient greffées après encapsulation dans un biomatériau sécurisant le système. Il est encourageant d'observer que les institutions américaines ont récemment dégagé d'importantes subventions de recherche sur la greffe d'îlot, laissant ainsi espérer une prochaine avancée thérapeutique pour cette maladie fréquente et invalidante.

